4.ライセンス制度システム利用方法(所持ライセンスの確認方法)
1.本制度について
- 慶應臨床研究ライセンス制度は、慶應義塾大学医学部の方針ならびに慶應義塾大学病院の理念及び臨床研究実施方針に沿った臨床研究・治験の積極的な推進のため、それらの実施に関わる教職員の資格を医学部・病院が認証することを目的として、2019年9月1日より施行されたものです。
- ライセンスの取得は慶應義塾大学医学部・病院臨床系研究に関する倫理審査委員会の申請要件となっております。
- 医学部・病院において臨床研究(本制度において、治験、特定・非特定臨床研究、再生医療等提供計画として行う臨床試験、人を対象とする生命科学・医学系研究などの臨床系研究を総称していいます)を実施する場合、臨床研究の種類および当該臨床研究における責任者または分担者としての立場に応じて、所定のライセンスを保持していることが求められます。
2.制度の概要
- 対象
- ライセンスの対象は慶應義塾大学医学部・病院で臨床研究を実施する方(有効なkeio.jpをお持ちの教職員)です。
- 管理
- ライセンスは慶應義塾大学病院 臨床研究教育研修 受講管理システム(以下、慶應CTR受講管理システムと表記)内の慶應臨床研究ライセンス制度システムのkeio.jpアカウントで管理しています。
*システムにはkeio.jp認証でログインします。
- ライセンスは慶應義塾大学病院 臨床研究教育研修 受講管理システム(以下、慶應CTR受講管理システムと表記)内の慶應臨床研究ライセンス制度システムのkeio.jpアカウントで管理しています。
- 取得順
- ライセンスはB→A→S→SPの順に取得する必要があります。
- 有効期限
- ライセンスの有効期限は取得日(合格日)より3年間です。
- 維持
- 取得したライセンスを3年間維持するためには、有効期限内に年1回の「ライセンス継続研修」(無料)を受講・修了する必要があります。
- 更新
- ライセンスは3年に1回、有効期限が切れる前に「ライセンス研修・認定試験」(有料)を受講・修了して更新する必要があります。
*ライセンスの取得・継続研修・更新については、以降の各項目にて詳細をご確認ください。
*「ライセンスの種類と各研究における役割」、「ライセンスの取得~維持~更新までの流れ」については下図をご参照ください。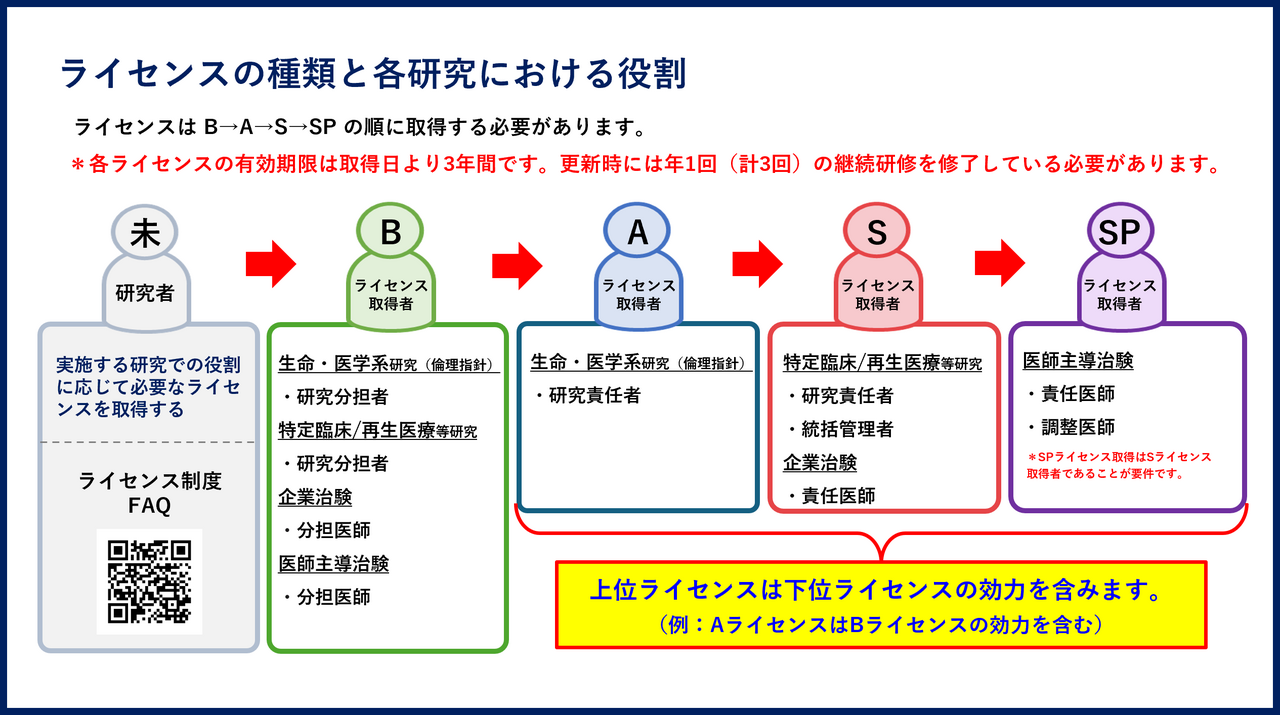
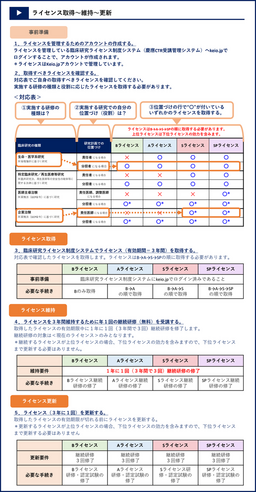
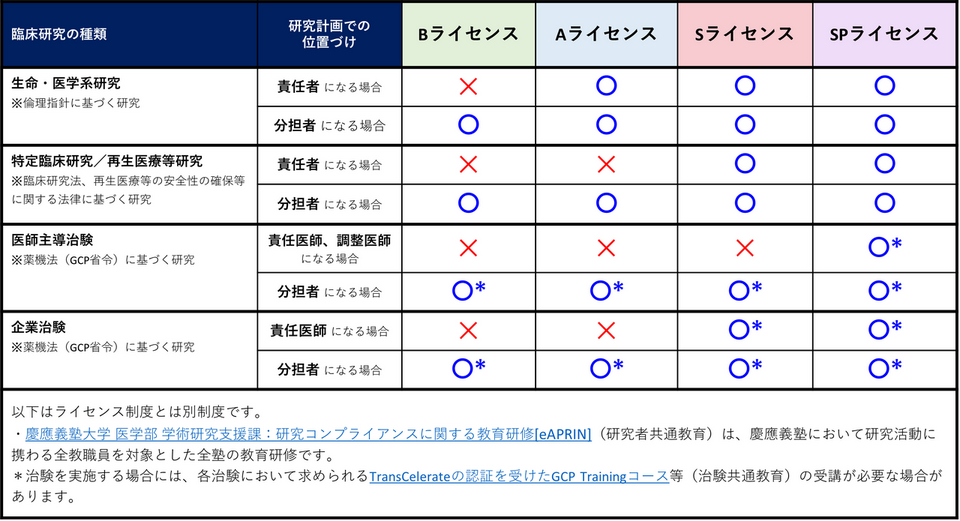
3.ライセンスの種類
- Bライセンス
- 法律及び倫理指針に基づいて行われる治験・臨床研究を、責任者以外(治験分担医師、研究分担医師、研究分担者など)として実施することを認証するライセンスです。
- Aライセンス
- 人を対象とする生命科学・医学系研究に関する倫理指針など、倫理指針の下で行われる臨床研究を、研究責任者ならびに実務責任者として実施することを認証するライセンスです。(Bライセンスの効力を含みます)
- Sライセンス
- 薬機法(GCP 省令)の下で行われる企業治験、ならびに臨床研究法、再生医療等安全性確保法など、法律の下で行われる臨床研究(先進医療や患者申出療養など、保険外併用療養費制度の下で実施される場合を含む)について、 責任者(治験責任医師、研究責任医師、統括管理者、研究責任者、実務責任者)として実施することを認証するライセンスです。(Aライセンス及びBライセンスの効力を含みます)
- SPライセンス
- 薬機法(GCP 省令)の下で行われる医師主導治験について、治験調整医師または治験責任医師として実施することを認証するライセンスです。(S ライセンス、A ライセンス及び B ライセンスの効力を含みます)
4.ライセンス制度システム利用方法(所持ライセンスの確認方法)
慶應義塾大学医学部・病院 臨床研究ライセンス制度のライセンスはkeio.jpアカウントで管理しており、ライセンスの取得・更新、継続研修の受講や取得ラ イセンスの確認などは慶應CTR受講管理システム内「慶應臨床研究ライセンス制度システム」で行います。慶應臨床研究ライセンス制度システムは、慶應CTR受講管理システムにkeio.jpアカウントでログインすることで利用できます。
*慶應義塾にご所属のkeio.jpをお持ちの方が対象です。
*システムを利用するためのユーザーアカウントは慶應CTR受講管理システムにkeio.jpでログインすると自動作成されます。
慶應臨床研究ライセンス制度システムへのログインはこちら(慶應CTR受講管理システム)
*システム利用の推奨環境はこちら
<システム利用案内>
<ログイン手順>※画面詳細
1.慶應CTR受講管理システムWebサイトにアクセスし、上部メニュー「ログイン」をクリック する。
*画面のスクロールでも [Login] メニューを表示できます。
2.[keio.jp Login]メニューの 「ログイン」 をクリックする。
3.keio.jp認証画面でkeio.jpメールアドレス(ID)とパスワードを入力し 「▶LOGIN」をクリックする。
3.ログインすると慶應臨床研究ライセンス制度システムメニューが表示されます。
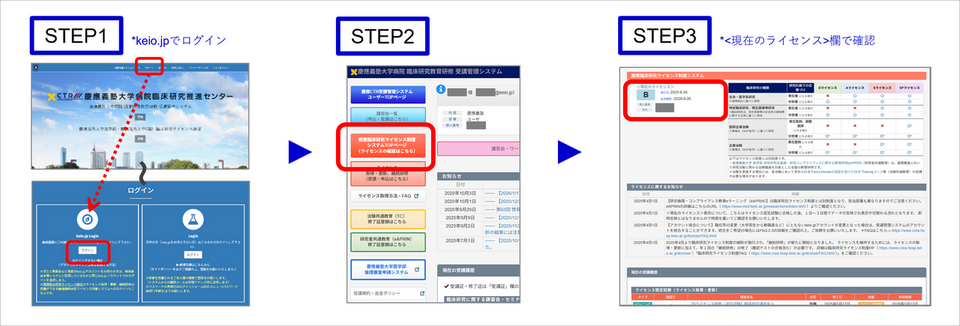
<所持ライセンスの確認手順>
1.慶應臨床研究ライセンス制度システム*にkeio.jpでログインする。[STEP1]
*慶應CTR受講管理システムのログインメニューよりログインします。
2.メインメニュー「慶應臨床研究ライセンス制度システムTOPページ(ライセンスの確認はこちら)」をクリックする。[STEP2]
3.慶應臨床研究ライセンス制度システムTOPページの<現在のライセンス>欄にて、ご自身が所持しているライセンス情報を確認できます。[STEP3]
*新たに取得したライセンス情報の反映はデータ処理の関係で1~3日かかることがあります。新規取得・更新したライセンスの確認は時間を置いてお試しください。
5.ライセンスの新規取得方法
ライセンスは慶應臨床研究ライセンス制度システムで「ライセンス研修・認定試験」を修了(合格)することで取得できます。各ライセンスの「ライセンス研修・認定試験」はライセンス研修eラーニングとWeb認定試験(有料)で構成され、システム上で随時受講可能です。なお、Bライセンスについては、年に2回実施している「臨床研究講習会(Bライセンス認定講習)」を修了することでも取得できます。
*ライセンスはB→A→S→SPの順に取得する必要があります。
|
Bライセンス |
Aライセンス |
Sライセンス |
SPライセンス |
|
|
事前準備 |
臨床研究ライセンス制度システムにkeio.jpでログイン済みであること |
|||
|
必要な手続き |
Bのみ取得 |
B→A の順で取得 |
B→A→S の順で取得 |
B→A→S→SP の順で取得 |
<ライセンス取得手順>
1.慶應臨床研究ライセンス制度システム*にkeio.jpでログインする。[STEP1]
*慶應CTR受講管理システムのログインメニューよりログインします。
2.メインメニュー「ライセンス取得・更新、継続研修(受講・申込はこちら)」をクリックする。[STEP2]
3.一覧よりご自身が取得すべきライセンス研修・認定試験の「詳細・申込」をクリックする。[STEP3]
4.詳細ページの教材欄に記載されているライセンス研修を受講する。
5.ライセンス認定試験(有料)へのお申込・支払後、試験を受け合格する。
6.合格するとライセンス(有効期限=合格日から3年間)が付与されます。
*新たに取得したライセンス情報の反映はデータ処理の関係で1~3日かかることがあります。新規取得・更新したライセンスの確認は時間を置いてお試しください。
➤慶應臨床研究ライセンス制度システム画面(クリックで拡大)※画面詳細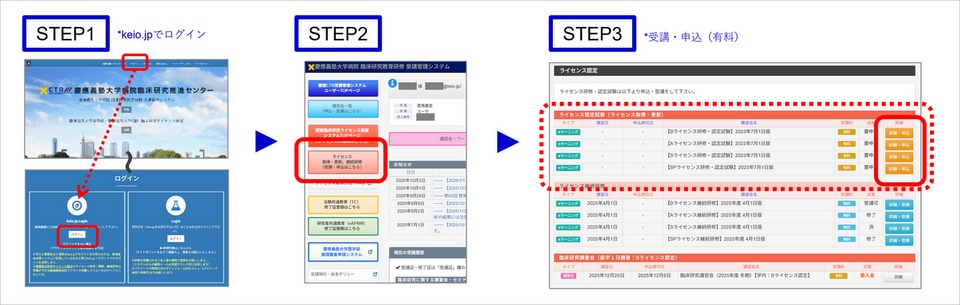
*研究倫理・コンプライアンス教育(eAPRIN)は慶應臨床研究ライセンス制度とは別制度となります(FAQ.7参照)。
*慶應臨床研究ライセンス制度「ライセンス研修・認定試験」は指針と臨床研究法に準拠しており、企業治験を実施する際に求められることが多いNPO法人TransCelerateのICH E6(R2)に対応したGCP Trainingコースの認証は受けておりません(FAQ.6参照)。
6.ライセンス継続研修の受講方法(ライセンスの維持)
2025年4月より、研究者が常に最新の情報を習得し、適正な臨床研究を実施するために継続研修の運用が開始されています。取得したライセンスを3年間維持するためには、ライセンスの取得後の有効期限内に年1回の「ライセンス継続研修」(無料)を修了する必要があります。なお、ライセンス更新(詳細は次項参照)には継続研修(無料)とライセンス研修・認定試験(有料)の2つを修了する必要があります。
*継続研修は3年に1回のライセンス更新(有料)とは別となりますので、ご注意ください。
|
Bライセンス |
Aライセンス |
Sライセンス |
SPライセンス |
|
|
維持要件 |
1年に1回(3年間で3回)継続研修の修了 |
|||
|
必要な手続き |
Bライセンス継続 |
Aライセンス継続 研修の修了 |
Sライセンス継続 研修の修了 |
SPライセンス継続 研修の修了 |
<ライセンス継続研修 受講手順>
継続研修の対象ライセンスは「慶應臨床研究ライセンス制度システムTOPページ」の<現在のライセンス>欄に表示されているライセンスです。
1.慶應臨床研究ライセンス制度システム*にkeio.jpでログインする。[STEP1]
*慶應CTR受講管理システムのログインメニューよりログインします。
2.メインメニュー「ライセンス取得・更新、継続研修(受講・申込はこちら)」をクリックする。[STEP2]
3.一覧より維持したいライセンスの継続研修「詳細・受講」をクリックする。[STEP3]
4.詳細ページの教材欄に記載されているライセンス研修を受講する。
5.確認テスト(無料)を受け、合格する。
➤慶應臨床研究ライセンス制度システム画面(クリックで拡大)※画面詳細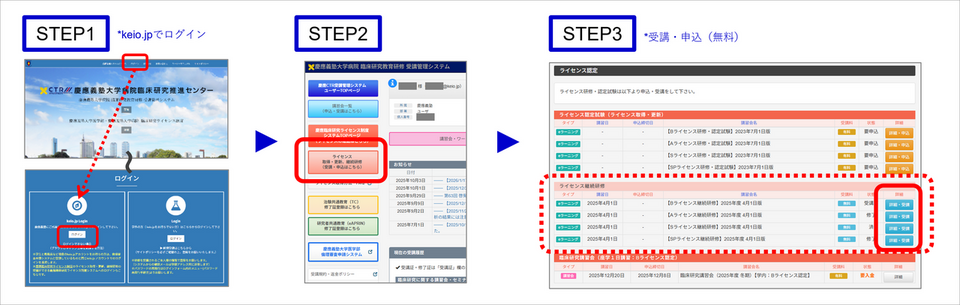
7.ライセンスの更新方法
ライセンスを更新する場合は、「ライセンス研修・認定試験」(有料)を3年に1回受講・修了する必要があります。なお、ライセンス更新の際には継続研修(前項参照)とライセンス研修・認定試験の2つを修了する必要があります。
*「ライセンス継続研修」(無料)はライセンスを維持するための研修で、継続研修のみでライセンスの更新はできません。
|
Bライセンス |
Aライセンス |
Sライセンス |
SPライセンス |
|
|
更新要件 |
継続研修 3回修了 |
継続研修 3回修了 |
継続研修 3回修了 |
継続研修 3回修了 |
|
必要な手続き |
Bライセンス 研修・認定試験の |
Aライセンス |
Sライセンス研 |
SPライセンス研 |
<ライセンス更新手順>
1.慶應臨床研究ライセンス制度システム*にkeio.jpでログインする。[STEP1]
*慶應CTR受講管理システムのログインメニューよりログインします。
2.メインメニュー「ライセンス取得・更新、継続研修(受講・申込はこちら)」をクリックする。[STEP2]
3.一覧より今回更新するライセンス研修・認定試験の「詳細・申込」をクリックする。[STEP3]
4.詳細ページの教材欄に記載されているライセンス研修を受講する。
5.ライセンス認定試験(有料)へのお申込・支払後、試験を受け合格する。
6.合格するとライセンス(有効期限=合格日から3年間)が付与されます。
*新たに取得したライセンス情報の反映はデータ処理の関係で1~3日かかることがあります。新規取得・更新したライセンスの確認は時間を置いてお試しください。
➤慶應臨床研究ライセンス制度システム画面(クリックで拡大)※画面詳細
8.内規・細則
- 慶應義塾大学医学部・病院 臨床研究ライセンス制度 内規【要Keio.jp認証】
- 慶應義塾大学医学部・病院 臨床研究ライセンス制度に関する細則【要Keio.jp認証】
9.お知らせ
以下のお知らせをご覧ください。
- 慶應で臨床研究に携わるには(2026/4/1)
- 臨床研究ライセンス制度 継続研修開始のお知らせ(2026/4/1)
- 臨床研究ライセンス制度 ライセンス研修・認定試験リニューアルのお知らせ(2023/6/21)
- 暫定ライセンスから正規ライセンスへの移行について(2022/6/20)
- 臨床研究ライセンス制度の一部改正について(2021/2/17)
- 臨床研究ライセンスの取得・更新について(補足)(2020/02/20)
- 臨床研究ライセンス制度の運用について(2019/11/18)
10.FAQ(よくあるご質問)
臨床研究ライセンス制度事務局では、正確に質問内容を把握し適切な回答を行うため、また経緯の記録・部内情報共有のため、電話での対応は控えさせていただいております。ご了承ください。
※ご質問の際は、FAQ掲載内容をあらかじめご確認下さい。
・「領収書 発行」申請
・「アカウント統合」申請
・「Bライセンス研修特別措置」申請
・「ライセンス取得証明書 発行」申請
2026年4月1日